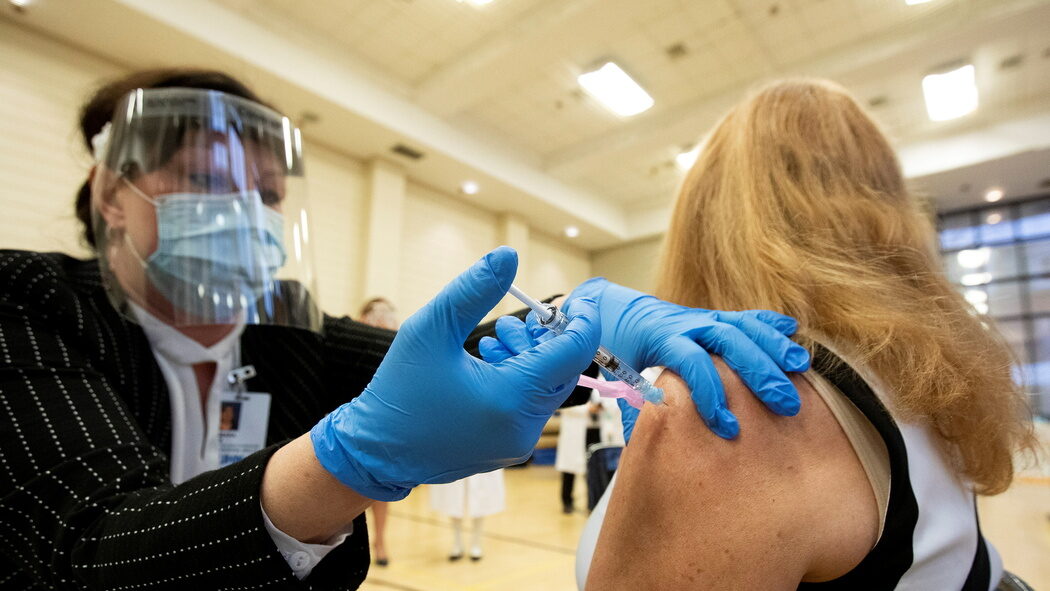
Zatím první prokázaný případ nákazou virem SARS-CoV-2 se v Číně objevil v listopadu 2019. Od té doby se covid-19 rozšířil doslova do celého světa a způsobuje bezprecedentní globální zdravotní, ekonomické, ale i psychické škody. Uplynulo dvanáct měsíců a v některých zemích se proti němu již očkuje. Jak je to možné, když vývoj nové očkovací látky trvá obvykle deset až patnáct let a stojí podle výrobců kolem jedné miliardy eur? Je taková vakcína bezpečná? Nezmění naši DNA? A proč vlastně Velká Británie nebo USA začaly s očkováním dříve než státy Evropské unie? Logické otázky, které ovšem mají i své odpovědi. Přečtěte si deset ověřených skutečností o vývoji a schvalování vakcín proti covid-19, které byste měli znát.
- Výzkum a vývoj očkovacích látek proti koronavirům a nových vakcinačních technologií probíhá již několik let. Globálně „mobilizované“ finance pak farmaceutickým firmám snižují vysoké riziko neúspěchu a mohou tak vývoj urychlit.
Vývoj jakékoli očkovací látky, která se má aplikovat zdravým lidem, je pečlivý, dlouhý a drahý. Výrobci udávají na jednu vakcínu obvykle 10 až 15 let a zhruba jednu miliardu eur. U vakcíny proti covid-19 však bylo možné navázat na předchozí výzkum a vývoj vakcíny proti onemocnění MERS, které známe od roku 2012 a také je způsobuje koronavirus. Nová technologie vakcíny využívající genetickou informaci viru je rovněž známa nejméně od roku 2011 z klinických zkoušek očkovacích látek proti rakovině.
Současný výzkum vakcíny proti covid-19 výrazně urychlila bezprecedentní „mobilizace“ peněz, ať již ze strany mezinárodních organizací jako Světová zdravotnická organizace (WHO) a Evropská unie, států, soukromých firem nebo globálních mecenášů jako je Nadace Billa a Melindy Gatesových. Ti vrhli do výzkumu a vývoje miliardy eur či dolarů bez ohledu na riziko neúspěchu a v naději, že alespoň „něco vyjde“. Farmaceutické firmy tak mohly značně zrychlit svůj postup a soustředit maximum svých odborníků i za cenu odložení jiných projektů a bez obav, že případný neúspěch přinese významné finanční ztráty. Všechny fáze vývoje – přezkum farmaceutické kvality, předklinický výzkum v laboratoři (in vitro) a na zvířatech (in vivo) a samotné klinické hodnocení u lidí – tak neprobíhají jako obvykle jedna za druhou, ale zčásti souběžně.